欢迎访问新医改评论 XYGPL.COM 您是第 3709354 位访问者

2002年,我国首部《药品管理法实施条例》正式公布,此后二十三年间虽历经3次局部修改,但原条例的制度框架与核心内容,已难以适应药品全生命周期监管的新要求。为此,国务院于2026年1月27日正式公布新修订的《中华人民共和国药品管理法实施条例》, 这是条例自施行以来的首次全面、系统性修订。修订后,条例框架结构由原10章80条调整为9章89条,修订条款占比超过90%,实现了监管制度的整体性重构与升级。
/01/修订背景:旧制度跟不上新实践
旧规则已无法适配新实践——这是修订《条例》最核心的动因,当 监管对象、产业形态、商业模式、临床需求乃至监管技术 均已发生深刻变化,只有通过系统性重构,才能筑牢药品安全底线,托举产业高质量发展。

/02/历史沿革:四次修订,一次重构
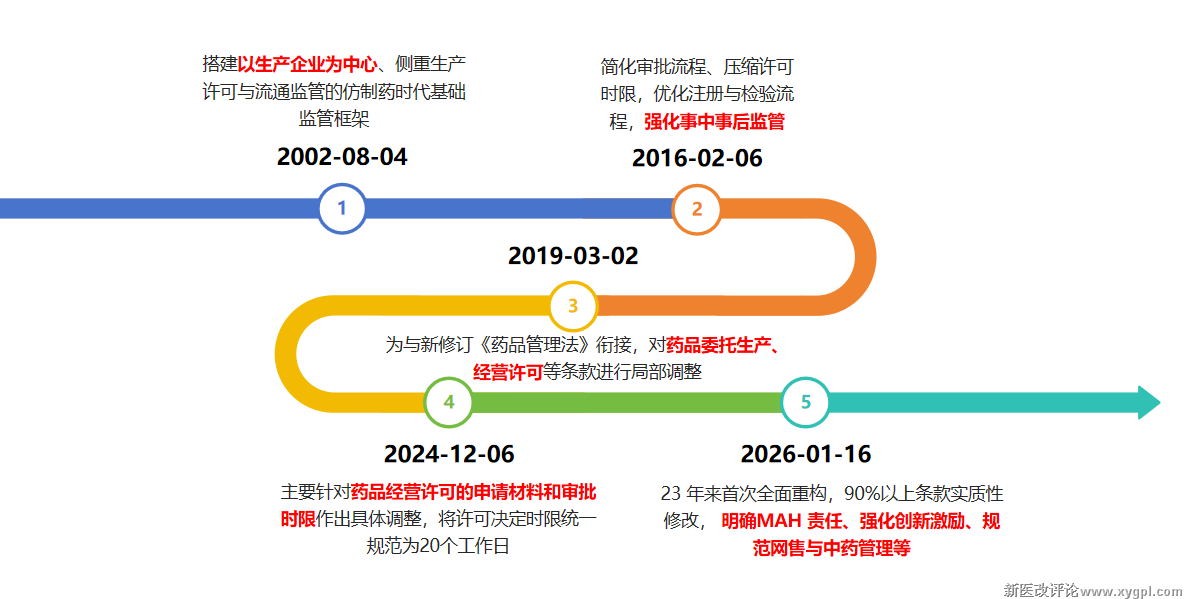
《中华人民共和国药品管理法实施条例》自2002年颁布以来,历经多次修订,以下是其历史沿革变化:
/03/重点变化:向“法定权利体系”的根本性转型
2002 年版《条例》以仿制药管理为基础,重点围绕生产许可与流通环节实施管理;2026 年新版《条例》则完成了从“行政许可体系”到“法定权利体系”的根本性转型:

通过 明确 MAH责任固化、创新保护多层化、生产模式灵活化、网络销售规范化和中药管理分类化 ,构建起适配我国医药产业由“仿制驱动”转向“创新驱动”发展的现代化药品监管体系。
/04/创新提速:加速药物研发,推动产业升级
1. 创新激励——提供最直接的动力和回报保障
· 构建以临床价值为导向的创新激励体系 ,通过设立市场独占期与数据保护期,引导企业竞争焦点从低水平价格战、营销战转向高水平研发创新与临床价值创造,从源头推动产业向创新转型。
2 . 监管核心——重塑产业主体与责任模式
· 解放研发活力 : 允许研发机构、科学家团队作为MAH持有药品批文 ,无需自建工厂,确立创新成果可持有、可转化、可商业化的法定权利体系,激活研发机构与创新主体活力。
· 强化质量保障: 倒逼所有企业 必须建立高水准的质量体系 ,推动整个产业从“粗放式生产”迈向 “精细化、合规化制造”。
3 . 生产管理——突破行业瓶颈,释放创新产能
创新药分段委托生产,让中国创新药企 可在全球范围内配置优质生产资源、聚焦核心研发 ,有效降低创新产业化门槛,支持创新主体轻资产、高效率发展,构建更高效灵活的现代医药产业生态。
4.中药管理——特色创新赛道
通过构建中药全链条、标准化、可追溯的管理体系,推动中药产业更基于 “临床证据、质量可控、工艺创新” ;鼓励运用新技术、新工艺开发改良型新药,为中药产业开辟了独特的现代化发展路径。
/05/总结
距2026年5月15日新《条例》正式实施仅剩最后两个月。对于医药企业而言,这不仅是法规过渡的缓冲期,更是主动适配新规则、抢占合规先机的关键窗口。能够围绕MAH责任落实、创新药研发布局、药品追溯体系建设和网络销售等领域提前部署,确保在新规落地时平稳过渡。
随着《条例》的深入实施,中国医药产业将加速向创新驱动的高质量发展模式转型,创新药研发与成果转化效率显著提升,中药现代化持续推进,行业整体向更规范、更高效、更具全球竞争力的现代化产业体系加速升级。
|
|
||||
相关文章