欢迎访问新医改评论 XYGPL.COM 您是第 3758377 位访问者

2026年4月14日,国务院办公厅正式发布《关于健全药品价格形成机制的若干意见》(国办发〔2026〕9号)。距离2025年2月的征求意见稿,已经过去了一年多。
这不是一次简单的“转正”。从“医保局发文”到“国务院办公厅发文”,从“完善”到“健全”,从“2027年成熟定型”到不再设定时间表——变化之多、调整之大,值得每一个医药从业者逐字逐句研读。
本文将按照正式文件的结构,逐段、逐句、逐字对比征求意见稿,分析每一处变化背后的政策逻辑,并提炼出对创新药企、仿制药企、商业保险公司等不同主体的核心影响。
1、第一部分文件定位于总体要求
解读:
总体要求的变化可以概括为“一升一降一删”。“升”的是发文层级——从医保局到国务院,政策权威性跃升;“降”的是语气强度——从“着力构建”到“有效服务”,从“成熟定型”到不再设定时间表,更加务实;“删”的是具体时间节点和冗长原则阐述,让文件更加简洁。
敲黑板了:删除2027年时间表,并不意味着政策不急,而是意味着政策制定者认识到药品价格形成机制的复杂性,不愿意为了赶进度而牺牲质量。这对企业来说,意味着政策调整的节奏会更加可预期,不会出现“大跃进”式的突变。
2、第二部分 完善重点环节药品价格政策
正式文件将征求意见稿“二、发挥市场决定性作用”和“三、增进市场公平竞争”整合为“二、完善重点环节药品价格机制”,结构更紧凑,逻辑更清晰。
(一)优化创新药等新上市药品首发价格机制
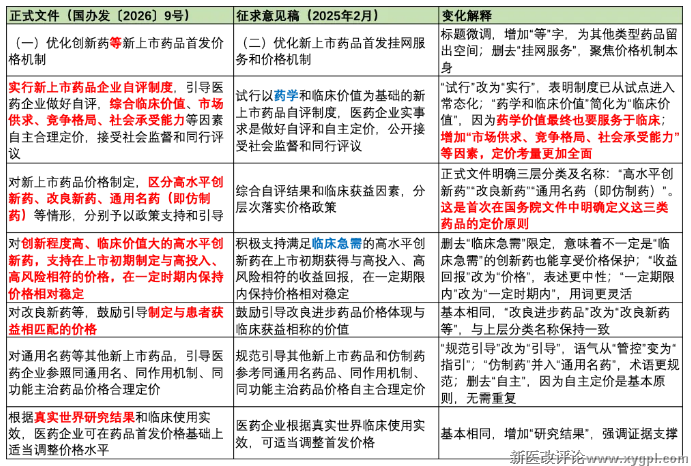
解读:
首发价格机制是本次文件的核心亮点之一。正式文件明确了“高水平创新药——改良新药——通用名药”三层分类定价框架,这是首次在国务院层面系统阐述这一逻辑。
敲黑板了:对于高水平创新药,“在一定时期内保持价格相对稳定”这一原则被保留。虽然正式文件没有像此前《新上市化学药品首发价格形成机制》(征求意见稿)那样明确写“1~5年”的稳定期,但“一定时期”的表述意味着保护期仍然存在,具体年限可能通过配套文件或实际操作中形成共识。
对于改良新药,“与患者获益相匹配”是一个相对模糊的标准。什么是“相匹配”?可能需要企业在自评中举证,也可能需要真实世界研究数据支撑。这意味着改良新药的定价将面临更严格的审查。
对于仿制药,“参照同通用名、同作用机制、同功能主治药品价格合理定价”——这意味着仿制药的定价空间将被已有药品的价格锚定,难以出现“独立定价”的情况。
(二)发挥医保支付标准对药品价格形成的引导作用
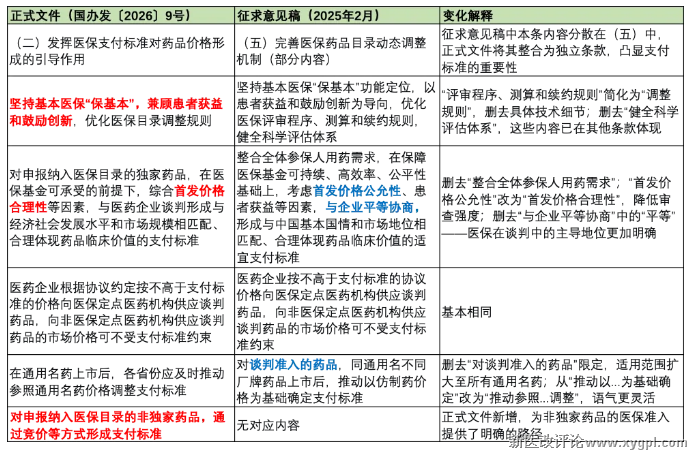
解读:
支付标准是医保引导药品价格的核心工具。正式文件在这一条款中做出了几个重要调整。
首先,删去了“与企业平等协商”中的“平等”二字,医保在谈判中的主导地位更加明确。
其次,扩大了支付标准调整的适用范围。征求意见稿中“对谈判准入的药品”的限定被删除,意味着所有通用名药上市后都可能触发支付标准的调整。这对原研药企业来说,意味着专利到期后的价格悬崖将更加陡峭。
第三,新增了非独家药品的竞价机制。这意味着未来非独家药品进入医保目录,将不再依赖个别谈判,而是通过竞价形成支付标准——这实际上是集采逻辑在医保准入环节的延伸。
(三)健全药品集中带量采购价格形成机制
解读:
集采条款的变化不大,说明集采政策已经相对成熟。值得关注的是新增的“加强对地方集中带量采购工作的指导”——近年来,部分地区在集采执行中出现了一些问题,如围标串标、非理性竞价等。正式文件强调“指导”和“保障质量供应稳定”,说明政策重心正从“扩面”转向“提质”。
四)完善药品挂网价格管理
解读:
挂网管理条款的核心变化是“加快建设”替代“统一建立”,以及“完善动态调整制度”替代“探索建立”。这说明政策制定者认识到,省级平台的建设和价格的动态调整不是一蹴而就的,需要给予时间和空间。
敲黑板了:“推动参比制剂、通用名药体现合理价格梯度”——这意味着原研药(参比制剂)和仿制药之间的价差将被引导缩小。这对原研药企业来说是一个需要关注的信号。
3、第三部分 推动相关主体发挥药品价格发现作用
正式文件将征求意见稿“四、鼓励经营主体参与价格形成”改为“三、推动相关主体发挥药品价格发现作用”,从“鼓励”变为“推动”,语气更强;从“参与”变为“发挥...作用”,定位更清晰。
五)发挥医疗机构专业作用
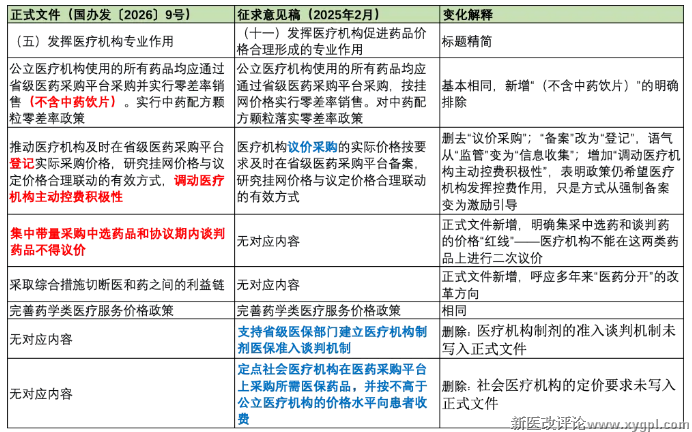
解读:
医疗机构条款的变化最为集中。正式文件新增了“集采中选药和谈判药不得议价”的规定,这是对近年来部分医疗机构二次议价行为的明确回应。同时,删去了征求意见稿中“议价采购备案”的强制要求,改为“登记实际采购价格”——这意味着政策层面对二次议价的支持力度减弱,挂网价的“锚定”作用将更强。
敲黑板了:对于药企来说,这是一个积极信号。过去,部分地区医疗机构在省级挂网价基础上进行二次议价,实际上形成了“挂网价是上限、议价后才是实际采购价”的局面。正式文件明确“不得议价”,意味着挂网价的执行力度将加强,药企的价格确定性将提高。
新增的“切断医和药之间的利益链”虽然是一句原则性表述,但出现在国务院文件中,意味着这一方向不会动摇。
(六)引导药店合理制定药品零售价格
解读:
药店条款的整体变化是语气从“管控”走向“引导”。“量价比较指数”从“构建”变为“编制”,“考核和处置”变为“评估”——这些变化表明,政策制定者认识到药店价格的形成主要靠市场竞争,行政干预的空间有限。通过公开比价、信息公开等方式引导价格合理,比强制降价更加可持续。
(七)用好网上药店价格发现功能
解读:
网上药店条款的核心变化是将平台的义务从“应加强...移交”变为“引导...报告”。这是一个重要的责任界定——平台不是执法机关,没有义务“移交”案件,只需要“报告”可疑情况即可。这符合平台经济的治理逻辑,也减轻了平台的合规负担。
4、第四部分 引导关键领域药品价格保持合理水平
正式文件将征求意见稿中分散的内容整合为独立章节“四、引导关键领域药品价格保持合理水平”,新增了“创新药多元支付”“麻精药品”“原辅料价格行为”等条款。
(八)促进创新药多元支付与价格合理形成
解读:
创新药多元支付条款是本次文件的重要亮点之一。正式文件将“研究建立丙类目录”升级为“加快商业健康保险创新药品目录落地实施”,表明这一工具已经从纸面走向实践。
敲黑板了:新增的“引入多方参与创新药价格协商”值得高度关注。这意味着创新药的价格形成机制将更加多元化——除了医保谈判,商保、慈善、企业等多方都可以参与价格协商。这对于那些医保支付标准较低、但仍有支付能力患者群体的创新药来说,是一个重要的政策空间。
但需要注意的是,丙类目录与医保目录的联动机制、进院渠道的具体要求等内容被删除,说明这些机制的落地仍需时间,不宜过早写入国务院文件。
(九)强化短缺药保供稳价
解读:
短缺药条款基本保留,核心机制未变。正式文件增加了“临床必需易短缺药品重点监测清单”,扩大了管理范围。短缺药议价通道的保留,为紧急情况下的药品供应提供了价格形成渠道。
(十)加强麻醉药品和精神药品价格管理
解读:
麻精药品条款新增了挂网价格上限的规定,明确“不得高于政府指导价或已报送的临时价格”。这是对麻精药品价格管理的进一步细化,防止企业利用信息不对称报出虚高价格。
(十一)规范药品原辅料价格行为
解读:
原辅料条款新增了“支持‘原辅料+制剂’一体化发展”,这是对近年来原料药垄断、断供问题的直接回应。当一家企业同时掌握原料药和制剂的生产,供应链的稳定性会大大提高,价格操纵的空间也会缩小。
中药材条款的变化值得关注——从“着力解决价格炒作问题”变为“加强价格引导,促进优质优价”。这说明政策制定者认识到,中药材价格问题的根源在于质量评价体系不完善,而不是单纯的“炒作”。只有建立了完善的质量评价体系,才能实现“优质优价”,从根本上解决价格乱象。
5、第五部分:加强药品价格治理
正式文件将征求意见稿“五、加强部门贯通协同”改为“五、加强药品价格治理”,聚焦价格治理本身,部门协同的内容移至新增的“六、加强组织实施”。
(十二)加强药品价格监测预警
解读:
监测预警条款基本保留。核心机制——以有效竞争形成的价格为基准进行风险提示——没有变化。这意味着未来价格监测的重点将是对“价格明显偏高”的药品进行提示和干预。
(十三)推进药品价格协同治理
解读:
价格协同治理条款新增了多个重要内容。“强化跨部门联合监管”和“加强政策协调衔接”体现了本次文件的核心理念——药品价格治理不是医保一个部门的事,需要多部门协同。
敲黑板了:“有效防范非理性竞价中标影响正常供应”是对集采中“自杀式报价”问题的直接回应。过去,部分企业为了中标报出低于成本的价格,中标后无法正常供应,影响了临床用药。正式文件明确要防范这一问题,意味着未来的集采规则可能会对报价的“合理性”有更多考量。
新增的“加强医药领域全链条穿透式审计监督”也是一个重要信号。近年来,医药领域的反腐力度不断加大,“穿透式审计”意味着监管将不局限于表面,而是追溯资金流向的每一个环节。
(十四)建立药品医保价值评估制度
解读:
医保价值评估条款的核心变化是将真实世界研究的范围从“丙类目录”扩展为“商业健康保险创新药品目录”。这与(八)中“加快商业健康保险创新药品目录落地实施”形成呼应——真实世界研究将为商保目录药品的价值评估提供证据支撑。
6、第六部分:加强组织实施
正式文件新增独立章节“六、加强组织实施”,征求意见稿中相关内容散见于“五、加强部门贯通协同”。
解读:
新增的“组织实施”章节是正式文件的重要变化之一。明确“医保部门要履行牵头职责”,同时强调“各地区要结合实际抓好贯彻落实”,表明政策制定者认识到“最后一公里”的重要性——文件再好,落不了地也是空文。
删去各部门职责的具体列举,并不意味着这些部门不重要。恰恰相反,药品价格形成涉及审评、生产、流通、使用、支付、监管等多个环节,任何一个环节的缺位都会影响政策效果。正式文件选择不详细列举,可能是为了避免“挂一漏万”,也可能是为了给后续配套文件留出空间。
7、总结
逐条对比完所有条款,有必要跳出细节,从战略层面提炼一下:这份文件到底变了什么?以下十个变化最值得关注——:
第一,政策层级跃升。 从医保局文件升级为国务院办公厅文件,权威性和执行力显著提升。这是第一份以国务院名义发布的、系统性的药品价格形成机制文件。
第二,删除2027年时间表。 不再设定“成熟定型”的具体时间节点,政策节奏更加从容务实,避免为了赶进度而牺牲质量。
第三,明确三层分类定价。 “高水平创新药——改良新药——通用名药”的分类框架首次写入国务院文件,不同层级适用不同的定价原则。
第四,创新药价格保护期保留但未明确年限。 “在一定时期内保持价格相对稳定”的原则保留,但未写具体年限。
第五,集采中选药和谈判药不得议价。 这是对二次议价的明确限制,对药企是一个积极信号——挂网价的执行力度将加强。
第六,议价备案改为登记。 医疗机构议价采购的强制备案要求被删除,改为“登记实际采购价格”,政策层面对二次议价的支持力度减弱。
第七,商保药品目录从“研究建立”到“加快落地”。 商保药品目录的推进节奏加快,但具体机制(如与医保目录联动、进院渠道等)未写入正式文件,留待配套文件明确。
第八,引入多方参与创新药价格协商。 这是重要的新增内容——创新药价格不再只是医保和企业之间的博弈。
第九,“原辅料+制剂”一体化发展获得政策支持。
第十,新增“防范非理性竞价中标”和“全链条穿透式审计监督”。 前者针对集采中的“自杀式报价”,后者针对医药领域反腐。
8、写在最后
这份正式文件与征求意见稿相比,不是简单的“转正”,而是经过了一年多深思熟虑后的“升级”。从“2027年成熟定型”到不再设定时间表,从“议价备案”到“不得议价”,从“研究建立丙类目录”到“加快落地”——每一处变化都有其政策逻辑。
对于创新药企,政策释放的信号是清晰的:高水平创新药的价格保护原则没有动摇,多元支付渠道正在加速构建,但定价需要接受更透明的社会监督和同行评议。
对于仿制药企,信号同样明确:价格锚定已成定局,竞争将更加激烈,但集采规则也在优化,“非理性竞价”将受到遏制。
对于商业保险公司,丙类目录从“研究”到“加快落地”意味着新的市场机会正在打开。
在医药行业从业多年,笔者见过医药政策的大起大落。
2015年之前,是“低水平重复”的时代,谁的批文多谁就厉害。2015年之后,是“审评审批改革”的时代,谁的质量好谁就厉害。2020年之后,是“集采+医保谈判”的时代,谁的成本低谁就厉害。
现在,我们正在进入一个新的时代——“临床价值+价格合理”的时代。
这个时代的特点是:政策不再“一刀切”,而是分层分类施策。高水平创新药有空间,低水平重复没有出路;真正解决临床问题的有价值,堆砌数据的没有意义。
这听起来很残酷,但其实很公平。正如乔治·默克所说:“药物是为人类而生产,不是为追求利润而制造的。只要我们坚守这一信念,利润必将随之而来。”这份文件,本质上就是在为这个信念搭建制度框架。
|
|
||||
相关文章