欢迎访问新医改评论 XYGPL.COM 您是第 3557702 位访问者

本期以表格形式对比解读"欧盟上市后监督重要概念":上市后监督计划、上市后性能跟踪、上市后临床跟踪、趋势报告、定期安全更新报告。
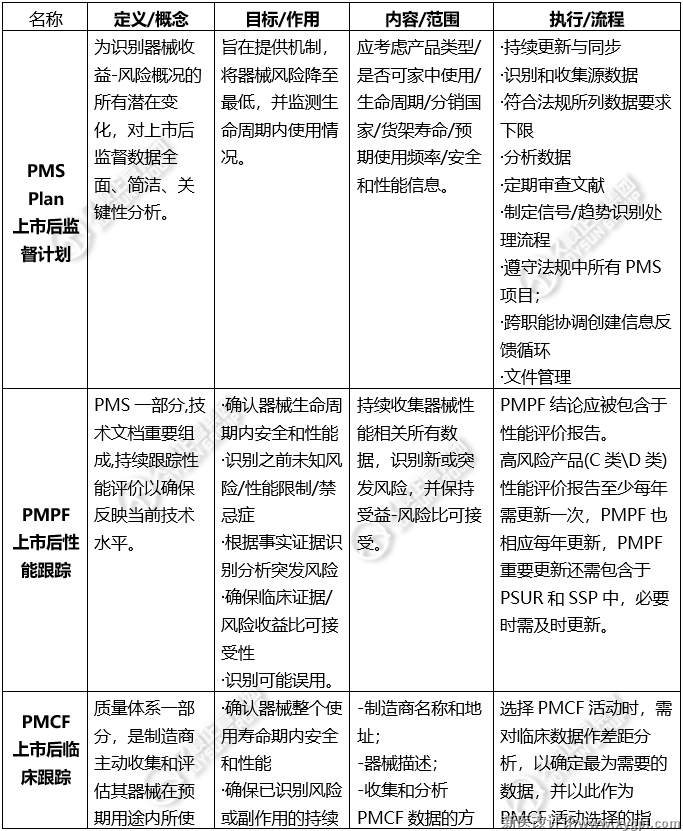
*PMS Plan上市后监督计划:为识别器械收益-风险概况的所有潜在变化,对上市后监督数据全面、简洁、关键性分析。
旨在提供机制,将器械风险降至最低,并监测生命周期内使用情况。
*PMPF上市后性能跟踪:PMS一部分,技术文档重要组成,持续跟踪性能评价以确保反映当前技术水平。
·确认器械生命周期内安全和性能
·识别之前未知风险/性能限制/禁忌症
·根据事实证据识别分析突发风险
·确保临床证据/风险收益比可接受性
·识别可能误用。
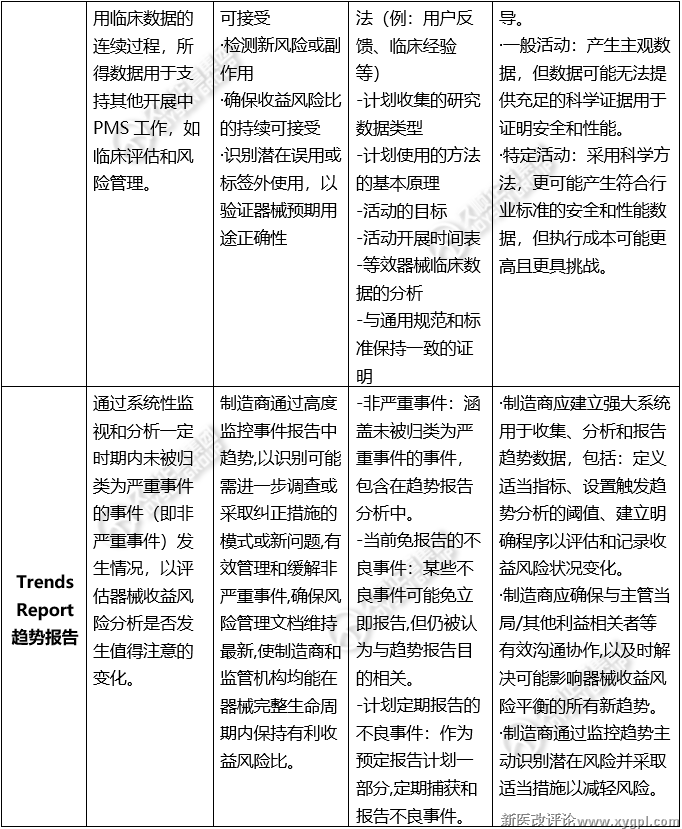
*PMCF上市后临床跟踪:质量体系一部分,是制造商主动收集和评估其器械在预期用途内所使用临床数据的连续过程,所得数据用于支持其他开展中PMS工作,如临床评估和风险管理。
·确认器械整个使用寿命期内安全和性能
·确保已识别风险或副作用的持续可接受
·检测新风险或副作用
·确保收益风险比的持续可接受
·识别潜在误用或标签外使用,以验证器械预期用途正确性
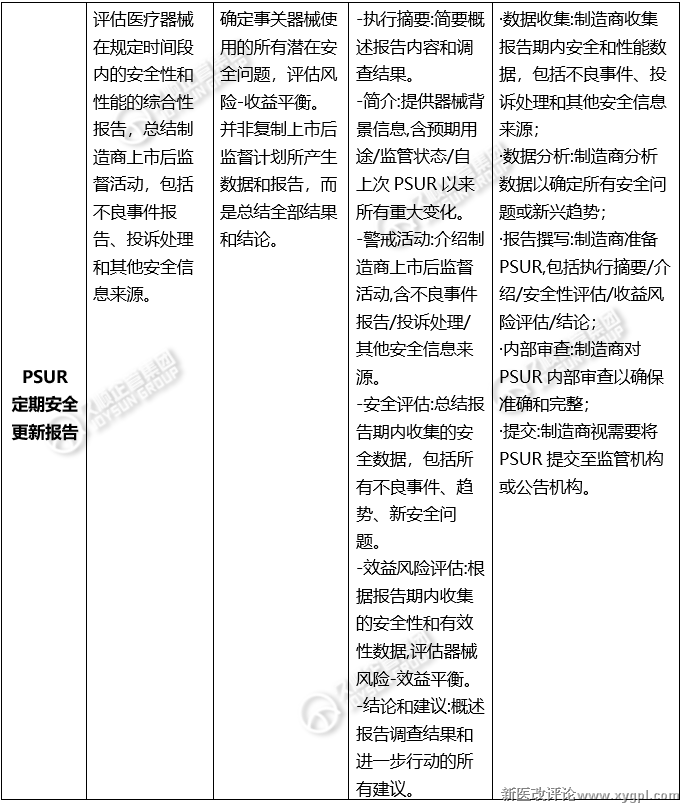
*PSUR定期安全更新报告:评估医疗器械在规定时间段内的安全性和性能的综合性报告,总结制造商上市后监督活动,包括不良事件报告、投诉处理和其他安全信息来源。
确定事关器械使用的所有潜在安全问题,评估风险-收益平衡。并非复制上市后监督计划所产生数据和报告,而是总结全部结果和结论。
*Trends Report趋势报告:通过系统性监视和分析一定时期内未被归类为严重事件的事件(即非严重事件)发生情况,以评估器械收益风险分析是否发生值得注意的变化。
制造商通过高度监控事件报告中趋势,以识别可能需进一步调查或采取纠正措施的模式或新问题,有效管理和缓解非严重事件,确保风险管理文档维持最新,使制造商和监管机构均能在器械完整生命周期内保持有利收益风险比。
|
|
||||
相关文章